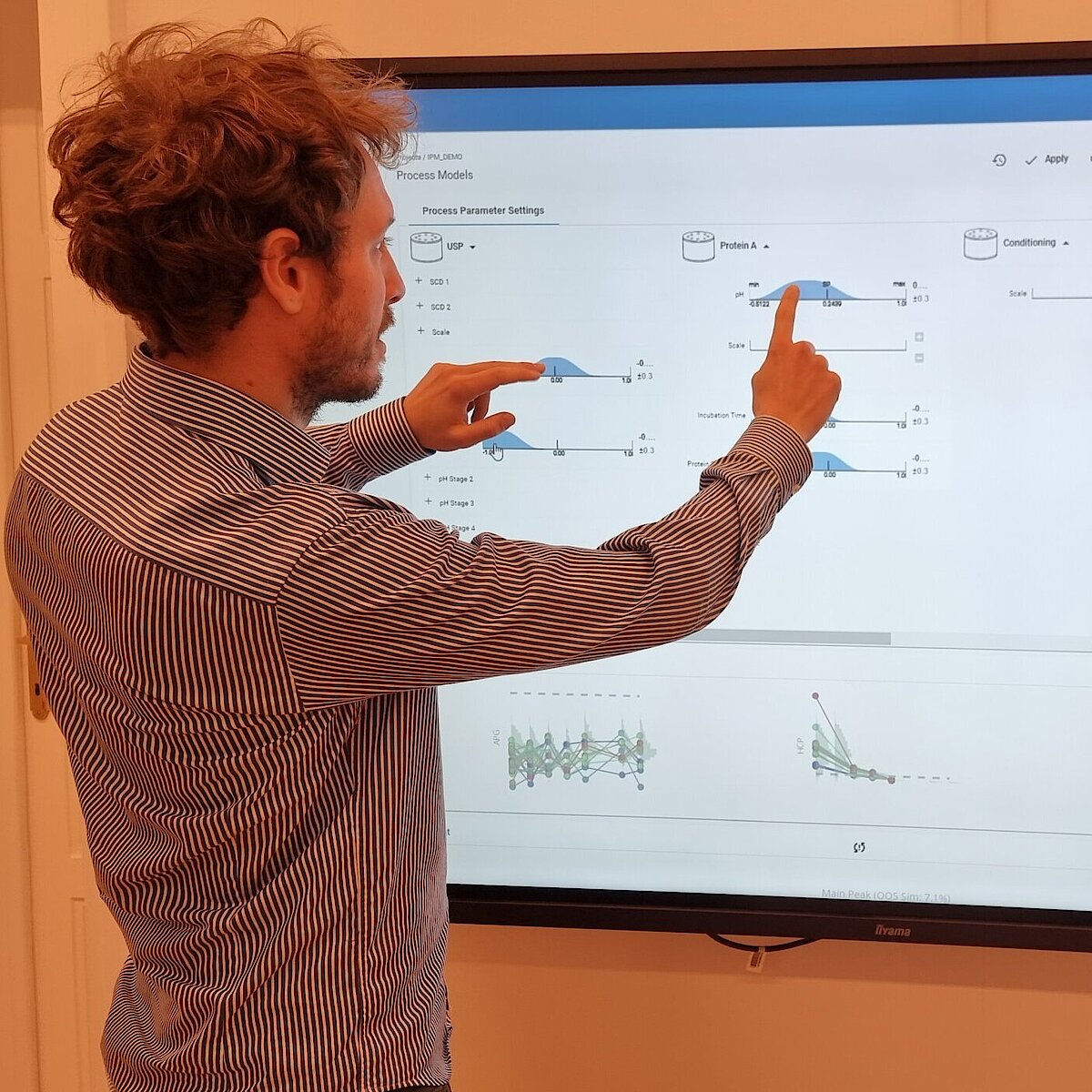
在制药行业的动态格局中,前沿技术的不断融合正在重塑行业标准。在这篇文章中,我们将揭示端到端数字孪生的开创性潜力,又称集成工艺模型(Integrated Process Models, IPM),它正在重新定义(生物)制药行业的未来。从提高生产灵活性到加快上市时间,我们将展示这些动态工具如何重新定义实时决策。此外,我们还探讨了通过将数字孪生与MES软件集成所实现的协同效应,从而为实时批次控制和批次放行创造机会。
Michael Grieves博士于2002年在密歇根大学首次定义了“数字孪生”的概念。在过去的几年里,“数字孪生”这个词在包括制药行业在内的许多行业引起了广泛关注。但数字孪生究竟是什么?它们又是如何彻底改变制药领域的?
现在对于“数字孪生”有很多定义,但其中一个特别能引起我们共鸣的定义是由IBM提出的[1]。根据其定义,数字孪生被描述为“某一对象或系统整个生命周期的虚拟再现,根据实时数据进行更新,并利用模拟、机器学习和推理来辅助决策。” IBM的观点强调,数字孪生不仅仅是大规模的模拟模型,而且是动态工具,可以不断从新数据中学习,预测未来的结果,并建议采取先发制人的行动——大大提高效率,降低风险,提高整体性能表现。
在工艺建模和生产数字化转型领域,工艺数字孪生既可以针对特定的单元操作专门设计,也可以针横跨整个生产过程的整体设计。本文将深入研究后一种方法,即端到端数字孪生或集成工艺模型(IPM) 在生物制药行业中的优势。
任何生物制药生产过程的目标都是不断尽可能地提高产量,同时持续稳定地保持产品功效和患者安全。这是由生产过程结束时的原液/制剂的质量来决定的。然而,生物制药生产过程通常由5~10个不同的单元操作组成。因此,如何将中间单元操作的执行效果与最终产品质量联系起来?如何确定对产品质量影响最大的单元操作,从而相应地分配更多资源?我们是否必须要求所有单元操作都具有相同精度的模型?这些关键问题只能采用一种整体方法来解决,该方法涵盖端到端的生产过程,将所有单元操作集成在一个统一的模型中。
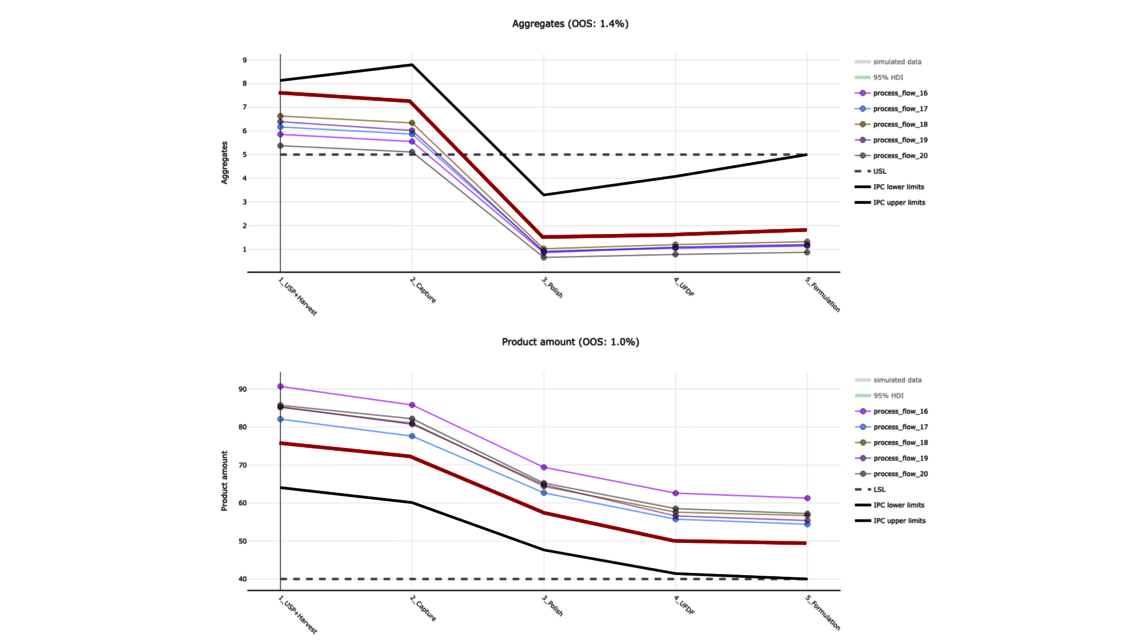
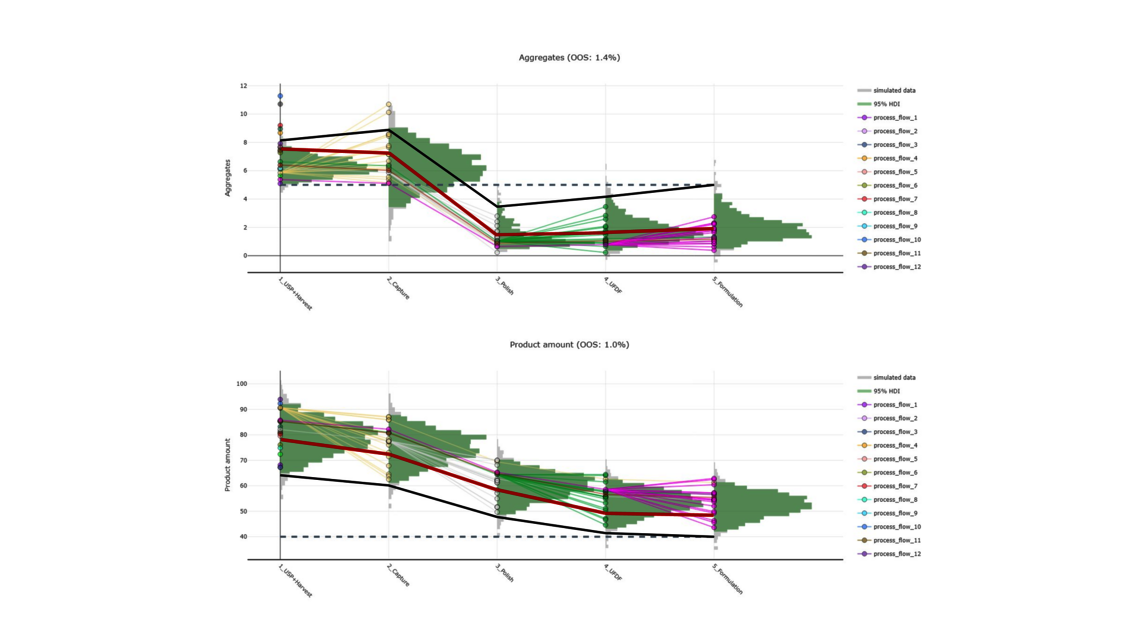
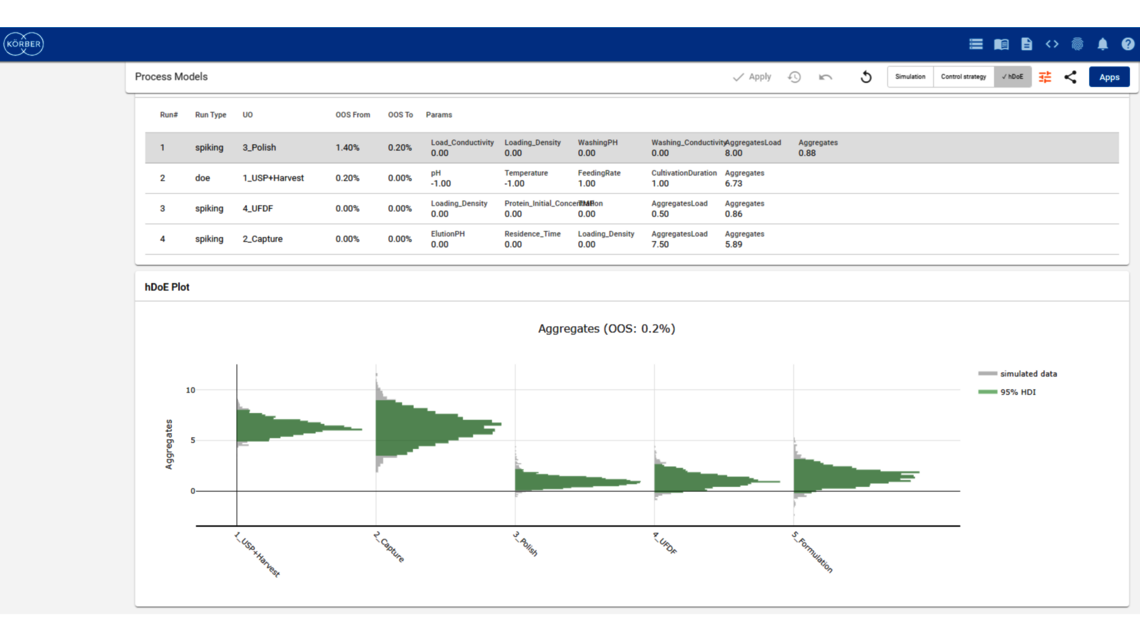
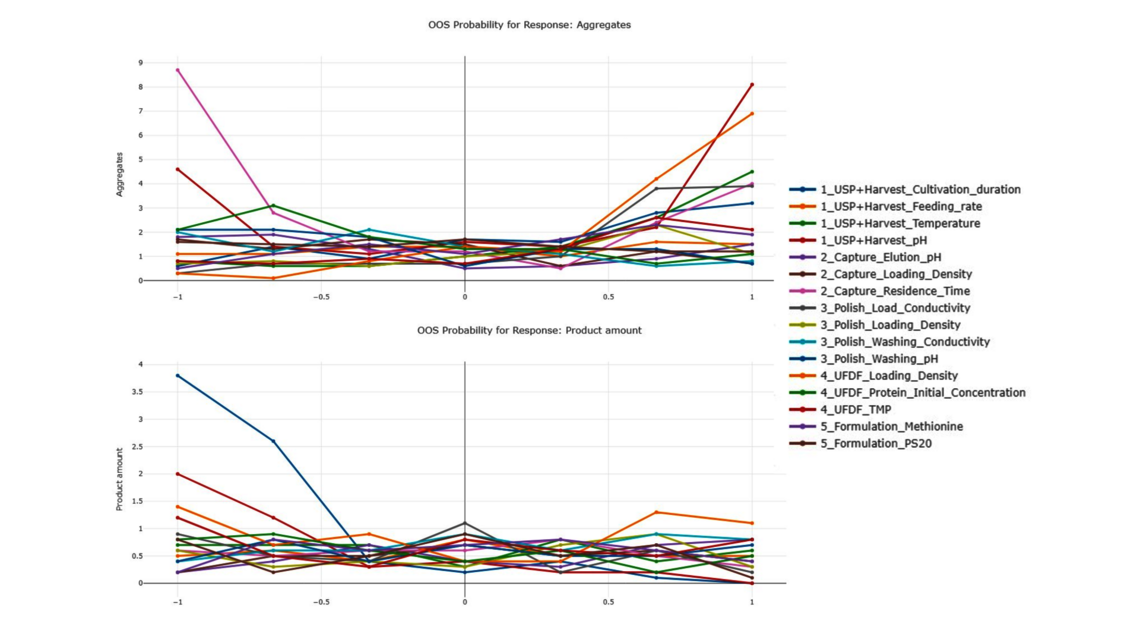
为了在这篇博文中展示端到端数字孪生的好处,我们将使用一个简化后的工业单克隆抗体(mAb)生产工艺的演示数据集。该数据集包括跨越5个不同单元操作(UOs)的5个大规模生产活动,以及基于实验设计方法(DoE)每1个单元操作进行15次实验,这是生物制药行业工艺验证第1阶段的常见数据集大小。我们将对两种响应进行建模:聚集体(关键质量属性,CQA)和产品量(关键绩效指标,KPI)。